实验介绍
本实验基于天然高分子材料丝素蛋白的结构特性,采用“脱胶—溶解—再生—自组装”这一方法论路径构建功能性纳米载药体系。首先在碱性条件下选择性去除丝胶以获得高纯度丝素纤维,随后通过 $\mathrm{CaCl_2:C_2H_5OH:H_2O}$ 三元溶剂体系破坏其高度有序的 $\beta$-折叠结构,实现分子尺度上的溶解与再生。在此基础上引入溶剂置换策略,通过调控体系介电环境诱导丝素蛋白发生构象转变与自组装,形成稳定纳米颗粒,并结合溶剂挥发过程实现结构固化。最终依托疏水作用与静电作用实现模型药物的有效负载,体现了从分子构象调控到介观结构构筑再到宏观性能实现的多尺度设计思想。
丝素蛋白的结构基础与提取原理
丝素蛋白提取原理
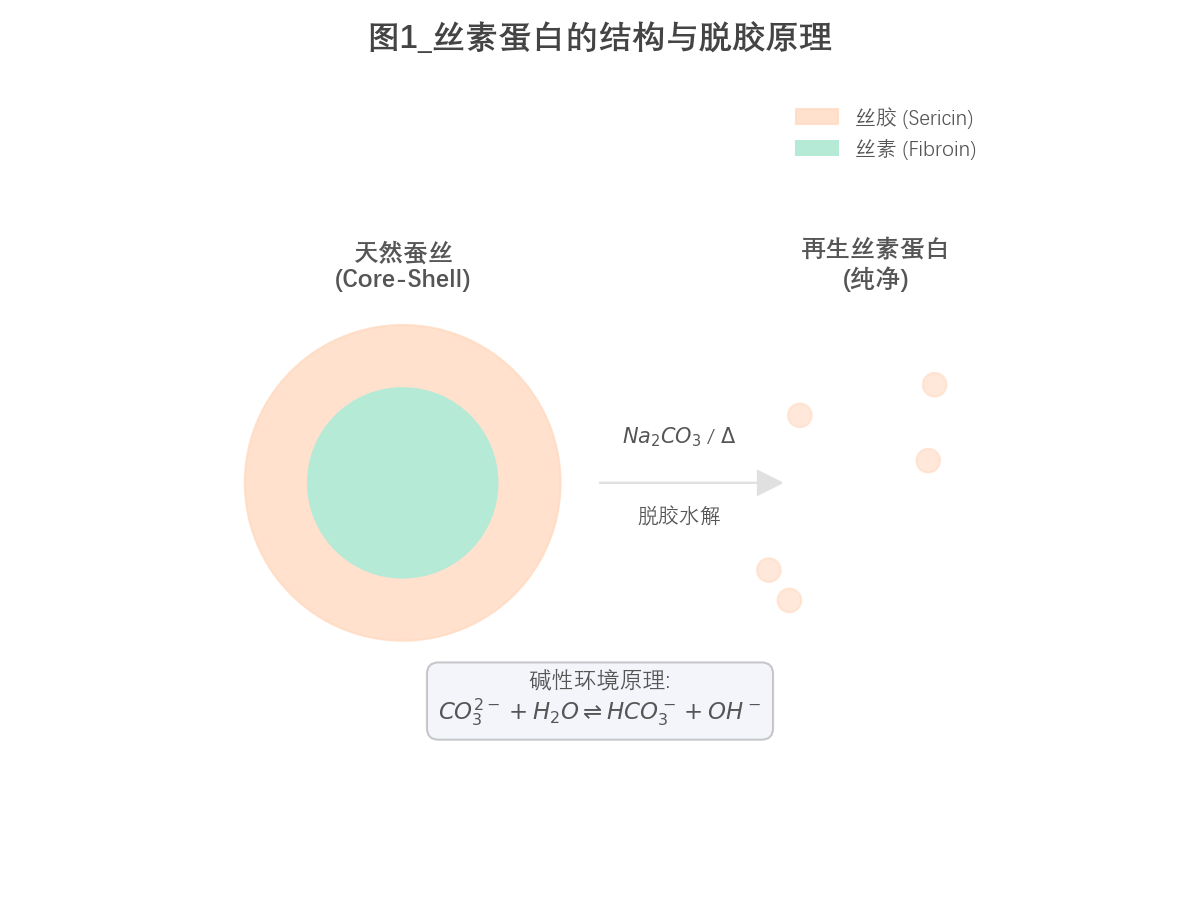
丝素蛋白来源于家蚕(Bombyx mori)蚕茧,蚕丝主要由约 70–80% 的丝素(Fibroin)和 20–30% 的丝胶(Sericin)组成。丝胶作为球状蛋白,富含极性侧基,易溶于热水或碱性环境,而丝素为高结晶度纤维蛋白,难溶于水。因此,本实验利用稀 $\mathrm{Na_2CO_3}$ 溶液在加热条件下提供弱碱环境,通过破坏氢键并引发部分肽键水解实现脱胶过程,其本质可表示为:
$$ \mathrm{CO_3^{2-} + H_2O \rightleftharpoons HCO_3^- + OH^-} $$
$$ \mathrm{R_1{-}CO{-}NH{-}R_2 + H_2O \xrightarrow{OH^-, \Delta} R_1{-}COO^- + H_3N^+{-}R_2} $$
脱胶后的丝素由于其稳定的 $\beta$-折叠结构难以直接溶解,需借助三元溶剂体系破坏分子间氢键及范德华力,使其由有序结晶态转变为无定形卷曲结构并溶解于水,随后通过透析去除无机盐,获得再生丝素蛋白溶液。
溶剂置换与自组装成核机理
自组装成核机理
丝素蛋白作为典型两亲性高分子,由疏水性结晶区(富含 Gly、Ala)与亲水性非结晶区共同构成。当向其水溶液中加入丙酮等水混溶性有机溶剂时,体系介电常数降低,引发去溶剂化效应,使分子溶解度下降并驱动体系向低吉布斯自由能状态转变。在此过程中,疏水链段(如 GAGAGS 序列)趋于内聚形成疏水核心,而亲水链段向外延展形成稳定外壳,从而构建胶束状纳米结构。同时,分子构象由无规卷曲或 $\alpha$-螺旋逐步转变为更稳定的 $\beta$-折叠结构,该结构作为物理交联点保证颗粒在水相中的稳定存在。
溶剂蒸发与颗粒固化
溶剂蒸发与固化
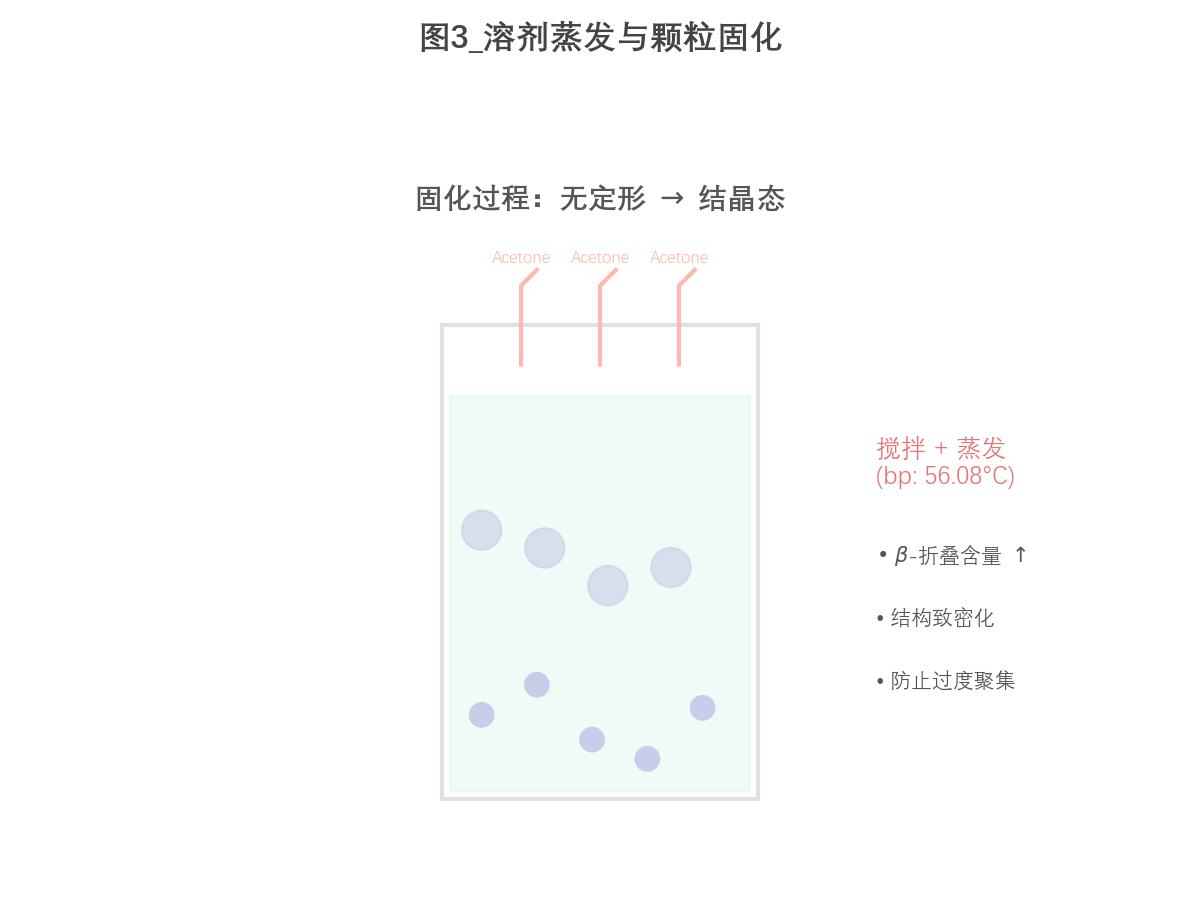
在纳米颗粒形成后,体系通过磁力搅拌促进丙酮逐步挥发,其沸点为:
$$ 56.08^\circ \mathrm{C} $$
显著低于水。随着丙酮去除,丝素分子间相互作用增强,$\beta$-折叠结构含量进一步提高,颗粒逐渐收缩并完成固化。该过程不仅实现有机溶剂去除,同时有效抑制颗粒间聚集,从而获得分散性良好的稳定纳米颗粒体系。
模拟药物(ICG)的负载机理
ICG负载机理
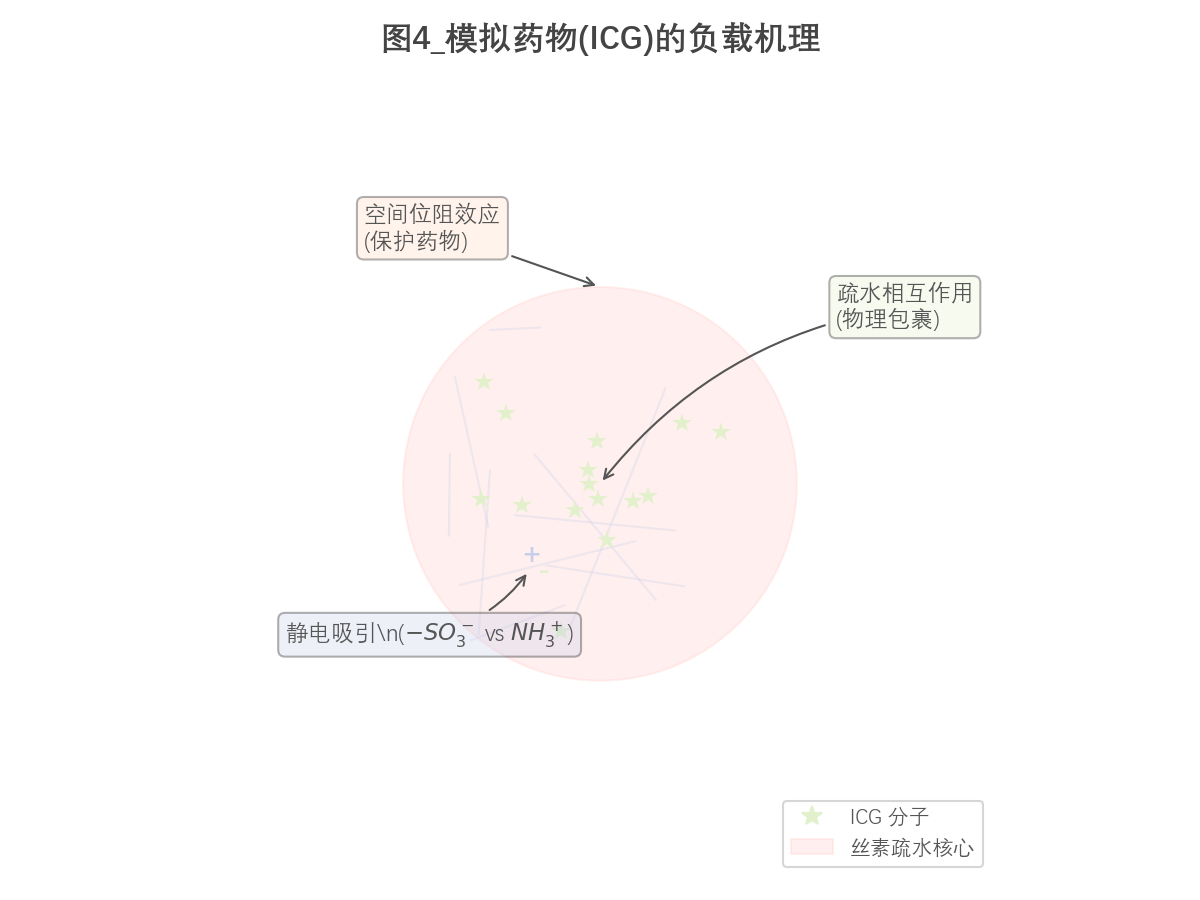
吲哚菁绿(Indocyanine Green, ICG)为典型两亲性三碳菁染料,在水溶液中易发生聚集与降解。在本体系中,其负载过程主要源于多重相互作用协同作用:首先,ICG 分子中的疏水芳香骨架倾向进入丝素蛋白内部疏水微区,实现物理包埋;其次,其磺酸基($-\mathrm{SO_3^-}$)所带负电荷可与丝素蛋白中带正电残基产生静电吸引,从而增强结合稳定性;此外,丝素蛋白形成的致密三维网络结构对 ICG 分子产生空间限域效应,使其有效隔绝外界光与氧化环境,从而提升体系整体稳定性。
实验指标分析
SF_ICG_Analysis_Dashboard
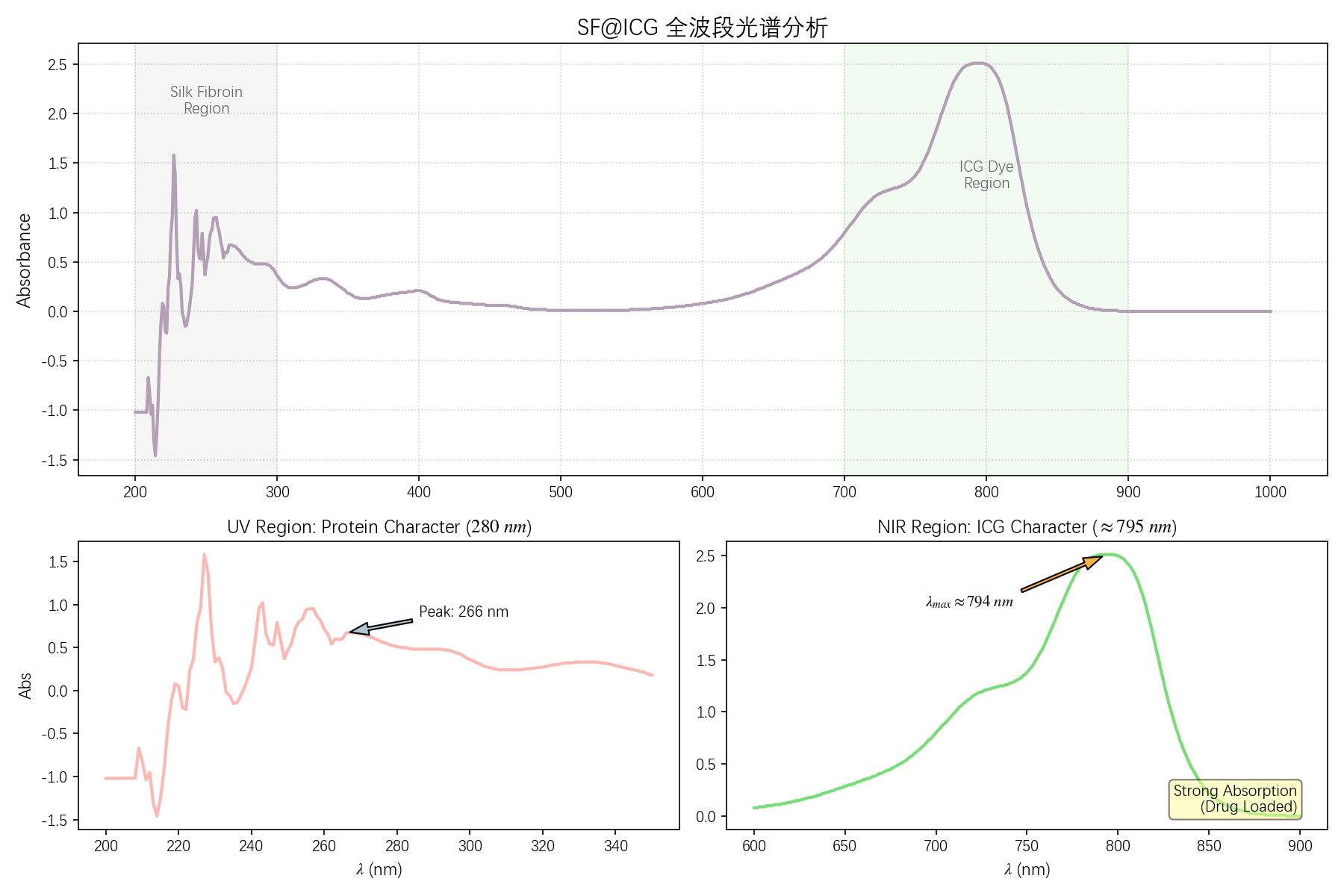
对 SF@ICG 纳米颗粒在 $200\text{–}1000\ \mathrm{nm}$ 范围内进行 UV-Vis 光谱分析,结果表明体系在紫外区与近红外区分别呈现丝素蛋白与 ICG 的特征吸收峰,且在 $>900\ \mathrm{nm}$ 区域基线回归零点,未出现明显散射拖尾,说明纳米颗粒在水相中具有良好的分散性且未发生显著团聚。
进一步分析可知,在紫外区(200–300 nm),$\lambda \approx 227\ \mathrm{nm}$ 处的强吸收源于肽键的 $n \rightarrow \pi^*$ 与 $\pi \rightarrow \pi^*$ 跃迁,而 $\lambda \approx 275\ \mathrm{nm}$ 附近的肩峰则来源于 Tyr、Trp、Phe 等芳香族氨基酸侧链的 $\pi \rightarrow \pi^*$ 跃迁。在可见-近红外区(600–900 nm),ICG 的最大吸收峰位于 $\lambda_{\max} = 795\text{–}798\ \mathrm{nm}$,相较于游离状态($\lambda_{\max} \approx 780\ \mathrm{nm}$)发生约 $15\text{–}20\ \mathrm{nm}$ 的红移。依据
$$ E = \frac{hc}{\lambda} $$
可知该红移对应电子跃迁能级降低,表明 ICG 分子处于丝素蛋白提供的疏水微环境中,从而验证其成功包载。
同时,在 $\lambda = 790\text{–}800\ \mathrm{nm}$ 区间内测得吸光度约为 $A \approx 2.51$,已超出仪器线性范围($0.1 < A < 2.0$)。根据比尔-朗伯定律
$$ A = \epsilon \cdot c \cdot l $$
可判断体系中 ICG 浓度较高,因此在后续定量分析中需进行适当稀释。综合离心纯化结果($12{,}000\ \mathrm{rpm}$)与光谱特征可知,样品在保留丝素蛋白特征峰的同时仍表现出显著 ICG 吸收及红移现象,表明 SF@ICG 纳米颗粒已成功构建,且药物稳定负载于载体内部,未发生明显流失。
作者:GARFIELDTOM
邮箱:coolerxde@gt.ac.cn